segunda-feira, 9 de março de 2009
Acantose nigricans

 A acantose nigricans é uma doença rara da pele, caracterizada pela presença de hiperqueratose (excesso de queratina) e hiperpigmentação (lesões de cor cinza e engrossadas, que dão um aspecto verrugoso ) e alopecia, principalmente nas pregas cutâneas perianais e nas axilas, mas que pode ocorrer em qualquer região mucocutânea.
A acantose nigricans é uma doença rara da pele, caracterizada pela presença de hiperqueratose (excesso de queratina) e hiperpigmentação (lesões de cor cinza e engrossadas, que dão um aspecto verrugoso ) e alopecia, principalmente nas pregas cutâneas perianais e nas axilas, mas que pode ocorrer em qualquer região mucocutânea.Conhecem-se quatro tipos de acantose nigricans:
* A síndrome de Miescher, que é uma forma benigna e hereditária;
* A síndrome de Gougerot Carteaud, que é também uma forma benigna e possivelmente hereditária, mas que aparece em mulheres jovens;
* A pseudo-acantose nigricans que é uma forma juvenil benigna que se associa a obesidade e alterações endocrinológicas.
* A acantose maligna, manifestação paraneoplásica do adulto que se associa com freqüência a um tumores do tubo digestivo e do fígado, bem como linfomas e melanoma.
Acrocianose
Acrocianose refere-se a uma doença vascular permanente que deixa a pele das mãos e, por vezes, dos pés com uma coloração azulada ou roxa (cianose), manifestando-se especialmente no inverno e em jovens mulheres. Outras características são a pele fria e úmida, possivelmente com aspecto pálido e inchaço. A cianose é associada a uma condição benigna que não requer intervenção médica; porém, quando não é benigna, pode indicar um sério problema médico, frequentemente acondicionada a outras doenças do tecido conjuntivo. (Não deve-se confundir acrocianose com doença de Raynaud, que se manisfesta por condições diferentes).
A acrocianose é vista também em pacientes com desordem neuro-hormonal crônica do sistema cardiovascular ou devido a um choque. Ou ainda, mais raramente, pode ser um sinal de uma doença, progressiva e lenta, como insuficiência cardíaca.
Sua manifestação ocorre em temperaturas entre 15 °C e 18 °C; e a coloração azulada deve-se a predominância de sangue pobre em oxigênio. E, embora não haja tratamento definitivo, pode-se amenizar, eventualmente, mantendo aquecida as extremidades do corpo.
Anemia
 Diz-se haver anemia (do grego, an = privação, haima = sangue) quando a concentração da hemoglobina sanguínea diminui aquém de níveis arbitrados pela Organização Mundial de Saúde em 13 g/dL para homens, 12 g/dL para mulheres, e 11 g/dL para gestantes e crianças entre 6 meses e 6 anos.
Diz-se haver anemia (do grego, an = privação, haima = sangue) quando a concentração da hemoglobina sanguínea diminui aquém de níveis arbitrados pela Organização Mundial de Saúde em 13 g/dL para homens, 12 g/dL para mulheres, e 11 g/dL para gestantes e crianças entre 6 meses e 6 anos.
O que é hemoglobina
A hemoglobina é o pigmento que dá a cor aos glóbulos vermelhos (eritrócitos) e tem a função vital de transportar o oxigênio dos pulmões aos tecidos.
Apesar de ter um cortejo de sintomas e sinais próprios, a anemia não é, em si, uma doença, mas uma síndrome, pois pode decorrer de uma extensa lista de causas.
É a síndrome crônica de maior prevalência em medicina clínica.
A anemia pode ser aguda ou crônica.
Na anemia aguda (perda súbita de sangue) a falta de volume no sistema circulatório é mais importante que a falta de hemoglobina. A perda de até 10% do volume sangüíneo, como a que ocorre numa doação de sangue, é bem tolerada. Perdas entre 10 e 20% causam hipotensão postural, tonturas e desmaios. Nas perdas acima de 20% há taquicardia, extremidades frias, palidez extrema, e hipotensão, depois choque; se a perda ultrapassar 30%, sem reposição imediata de líquidos intravenosos, o choque torna-se rapidamente irreversível e mortal.
Nas anemias crônicas não há baixa do volume sangüíneo, que é compensado por aumento do volume plasmático.
A falta de hemoglobina, como regra acompanhada de diminuição do número de eritrócitos, suas células carreadoras, causa descoramento do sangue, com palidez do paciente, e falta de oxigênio em todos os órgãos, com os sinais clínicos daí decorrentes. Hipócrates (@400 a.C.) descreveu-os: palidez e fraqueza devem-se à corrupção do sangue.
O sistema nervoso central, o coração e a massa muscular são os órgãos mais afetados, pois são os que mais necessitam oxigênio para suas funções.
A sintomatologia aumenta com a atividade física, pois esta consome oxigênio.
Com hemoglobina entre 9 e 11 g/dL há irritabilidade, cefaléia e astenia psíquica; nos velhos há fatigabilidade e podem ocorrer dores anginosa
Com hemoglobina entre 6 e 9 g/dL há taquicardia, dispnéia e fadiga aos menores esforços.
Com hemoglobina abaixo de 6 g/dL a sintomatologia está presente mesmo em atividades sedentárias e quando abaixo de 3,5 g/dL a insuficiência cardíaca é iminente e toda a atividade impossível.
As queixas espontâneas dos pacientes, entretanto, são menos exuberantes que a descrição acima: sem se aperceberem diminuem progressivamente a atividade física até níveis assintomáticos, e dizem nada sentir.
Diagnóstico
O hemograma é o exame fundamental para o diagnóstico da anemia. É feito, atualmente, em contadores eletrônicos de grande porte e alto preço (de US$80000 a US$400000), que contam e medem os eritrócitos e geram curvas de freqüência com médias e coeficientes de variação, definindo os parâmetros numéricos da população eritróide. As melhores máquinas distinguem e contam os eritrócitos mais jovens (reticulócitos), permitindo-se assim uma avaliação da produção diária e da resposta regenerativa à anemia.
Complementando-se os números dessa fantástica tecnologia com a observação ao microscópio por um patologista-clínico experiente, a grande maioria dos casos de anemia pode ser caracterizada quanto a seu mecanismo de produção (patogênese), o que leva ao diagnóstico da doença ou evento básico causal (etiologia). Deste modo:
| Quando a patogênese é a produção inadequada de hemoglobina, seja por falta de ferro ou por defeito genético na síntese, o hemograma evidenciará a presença de eritrócitos menores que o normal (microcitose), por faltar-lhes conteúdo. | |
| Nas anemias decorrentes de inibição da proliferação eritróide, como na falta de vitamina B12 , no uso de drogas antiblásticas (usadas no tratamento do câncer) ou em algumas doenças próprias da medula óssea, serão notados eritrócitos com volume médio superior ao normal (macrocitose). | |
| Nas anemias que acompanham as doenças crônicas, infecciosas, reumáticas, renais, endócrinas, o hemograma caracteriza-se “por não ser esclarecedor”; devem ser procurados os sinais clínicos e os resultados de exames próprios de cada uma delas. | |
| Nas anemias por excesso de destruição periférica dos eritrócitos (anemias hemolíticas) e nos dias que sucedem uma hemorragia, o hemograma mostrará aumento significativo dos reticulócitos, caracterizando a hiperregeneração reacional do tecido eritróide da medula óssea. |
Tipos de anemia
As anemias mais freqüentes e/ou de particular importância tanto médica quanto social são:
| Anemia da carência de ferro (anemia ferropênica) | ||
| Anemia das carências de vitamina B12 (anemia perniciosa) e de ácido fólico | ||
| Anemia das doenças crônicas | ||
| Anemias por defeitos genéticos: | ||
| - anemia de células falciformes | ||
| - talassemias | ||
| - esferocitose | ||
| - deficiência de glicose-6-fosfato-desidrogenase (favismo) | ||
| Anemias por agressão periférica aos eritrócitos: | ||
| - malária | ||
| - anemias hemolíticas imunológicas | ||
| - anemia por fragmentação dos eritrócito | ||
| Anemias decorrentes de doenças da medula óssea: | ||
| - anemia aplástica | ||
| - leucemias e tumores na medula |
Artrite psoriática
 A artrite psoriática é uma artrite inflamatória, geralmente soronegativa para o fator reumatóide, associada a psoríase cutânea. Não costuma ter predomínio de sexo, a não ser em subtipos específicos (predomínio do sexo feminino na forma poliarticular simétrica e do sexo masculino na forma espondilítica). Inicia‑se freqüentemente entre a terceira e quinta décadas de vida, sendo rara a artrite psoriática juvenil, que, quando se apresenta, tem como sintoma inicial à artrite assimétrica associada a dactalites, evoluindo posteriormente com acometimento cutâneo. Predomina em populações caucasóides. A psoríase cutânea é doença bastante freqüente, podendo acometer de 1 a 2% da população; em média, 5 a 10% dos pacientes com psoríase cutânea evoluirão com artrite psoriática.
A artrite psoriática é uma artrite inflamatória, geralmente soronegativa para o fator reumatóide, associada a psoríase cutânea. Não costuma ter predomínio de sexo, a não ser em subtipos específicos (predomínio do sexo feminino na forma poliarticular simétrica e do sexo masculino na forma espondilítica). Inicia‑se freqüentemente entre a terceira e quinta décadas de vida, sendo rara a artrite psoriática juvenil, que, quando se apresenta, tem como sintoma inicial à artrite assimétrica associada a dactalites, evoluindo posteriormente com acometimento cutâneo. Predomina em populações caucasóides. A psoríase cutânea é doença bastante freqüente, podendo acometer de 1 a 2% da população; em média, 5 a 10% dos pacientes com psoríase cutânea evoluirão com artrite psoriática.
Etiopatogenia - Não existe um antígeno de histocompatibilidade associado à artrite psoriática como um todo; o que vem sendo observado de maneira crescente é a tendência à associação entre subtipos de artrite psoriática e alguns HLA específicos. O HLA‑B 27 está comumente associado a forma axial, enquanto os HLA‑B 38 e B 39 são mais freqüentes nas formas periféricas da doença; o HLA‑DR 4 pode ser encontrado na forma poliarticular simétrica (AR-like) e o HLA‑A 2, nos casos de artrite psoriática juvenil.
Embora ainda existam muitas etapas a serem elucidadas na etiopatogenia da artrite psoriática, acredita‑se que, num indivíduo geneticamente predisposto, a presença de um fator ambiental possa funcionar como “gatilho” para desencadear as alterações imunológicas que darão origem a doença. Dentre os fatores ambientais, podemos citar infecção (retrovírus ou bactérias Gram-positivas, como o estreptococo) e trauma articular.
O estresse emocional representa importante papel no desencadeamento tanto da psoríase cutâneo quanto articular, porém os mecanismos neuroimunoendócrinos envolvidos neste processo ainda necessitam ser esclarecidos. Do ponto de vista imunológico, são observadas alterações tanto da imunidade humoral (produção de auto-anticorpos contra antígenos da derme e da membrana sinovial, e presença de imunocomplexos circulares), quanto da imunidade celular (subpopulações de linfócitos T ativados na pele e na membrana sinovial).
Quadro Clínico : - Na artrite psoriática, a lesão cutânea costuma preceder o quadro articular em 75% dos casos, havendo início simultâneo em 10% dos pacientes; nos restantes 15%, a artrite precede a psoríase cutânea. Não costuma haver correlação entre o tipo ou a gravidade da lesão cutânea e a presença, tipo ou extensão do quadro articular. Quando existe suspeita clínica de artrite psoriática e o paciente nega ter psoríase cutânea, convém procurar a lesão cutânea no couro cabeludo, em superfícies extensoras de grandes articulações (joelhos, cotovelos) ou na região umbilical. Alguns pacientes com oligoartrite assimétrica podem referir história passada de psoríase gutata ou história familiar positiva de psoríase.
Classicamente, a artrite psoriática apresenta cinco formas clínicas, tais como: Oligoartrite assimétrica (70%): é a forma clínica mais freqüente, acometendo grandes e/ou pequenas articulações. É comum a presença de tenossinovites, com os chamados “dedos em salsicha”. Poliartrite simétrica (15%): apresenta quadro articular muito semelhante a artrite reumatóide. Pode acometer as articulações interfalangianas distais, comumente não afetadas na artrite reumatóide. Distal (5%): acomete exclusivamente as articulações interfalangianas distais, geralmente associada a lesões ungueais (pequenas depressões circulares no leito ungueal, que demanda diagnóstico diferencial com micose ungueal).
Artrite mutilante (< class="hilite2">és, evoluindo para deformidades importantes, com encurtamento dos dedos. Espondilite (5%): o quadro clínico pode ser indistinguível daquele apresentado pela espondilite anquilosante. No entanto, costuma haver muitas diferenças radiológicas entre a espondilite psoriática e a espondilite anquilosante.
A artrite psoriática não costuma apresentar manifestações viscerais. Alguns autores costumam pleitear a inclusão da Síndrome SAPHO (acrônimo de Sinovite, Acne, Pustulose palmoplantar, Hiperostose esterno‑costoclavicular, Osteíte multifocal crônica recorrente) como um subtipo distinto da artrite psoriática. No entanto, o assunto está longe de ser uni consenso, aliado a extrema raridade da síndrome.
Nas formas clínicas periféricas da artrite psoriática, as alterações radiológicas são importantes no diagnóstico diferencial com a artrite reumatóide. Caracteristicamente, é observado, na artrite psoriática, destruição significativa de articulações isoladas, de maneira assimétrica. Nas articulações interfalangianas, é comum ocorrer osteólise da falange proximal (”ponta de lápis”) e alargamento da base da falange distal (”cálice invertido”). Por serem patognomônicas, quando a alteração tipo “ponta de lápis” e “cálice invertido” ocorrem num indivíduo sem psoríase cutânea, diz-se que este apresenta artrite psoriática sine psoríase.
A espondilite psoriática apresenta inúmeras diferenças radiológicas em relação a espondilite observada na espondilite anquilosante. A sacroileíte costuma ser unilateral ou bilateral assimétrica. Os sindesmófitos costumam ser assimétricos, irregulares, grosseiros, paramarginais, não acometendo todos os corpos vertebrais, em contraste a simetria absoluta da espondilite anquilosante.
Métodos de imagem mais sofisticados, como tomografia computadorizada, cintilografia óssea ou ressonância nuclear magnética, costumam ser desnecessários nos casos definidos de artrite psoriática.
Tratamento: Os antiinfiamatórios não hormonais são utilizados de rotina no tratamento da artrite psoriática, com evidente melhora da dor articular e sem provocar exacerbação das lesões cutâneas, mas não afetam a evolução da doença. Quanto aos corticosteróides, embora concorram para melhoria da dor e inflamação articular, estão associados a exacerbação da lesão cutânea no processo de retirada da droga, não é conveniente seu uso.
Não existe nenhuma droga de base que comprovadamente altere a evolução da artrite psoriática. Nos casos não responsivos aos AINH, a droga de primeira escolha é o metotrexato, na dose de 5 a 25mg semanal, por via oral ou intramuscular. A grande vantagem do metotrexato é sua ação tanto em nível cutâneo quanto articular. Nos casos mais leves, também podem ser utilizadas a sulfassalazina (1,0 a 3,0g/dia) e a hidroxicloroquina (400mg/dia), enquanto nos casos mais graves pode ser utilizada a azatioprina (100 a 150mg/dia).
Artrose
O que é?
É a doença articular mais freqüente e a cartilagem é o tecido inicialmente alterado. A cartilagem está aderida à superfície dos ossos que se articulam entre si. É formada por um tecido rico em proteínas, fibras colágenas e células.
Como se desenvolve?
A Osteoartrite (OA) tem início quando alguns constituintes protéicos modificam-se e outros diminuem em número ou tamanho. Há tentativa de reparação através da proliferação das células da cartilagem mas o resultado final do balanço entre destruição e regeneração é uma cartilagem que perde sua superfície lisa que permite adequado deslizamento das superfícies ósseas.
Este processo acompanha-se de liberação de enzimas que normalmente estão dentro das células cartilaginosas. A ação destas enzimas provoca reação inflamatória local a qual amplifica a lesão tecidual. Aparecem erosões na superfície articular da cartilagem que fica como se estivesse cheia de pequenas crateras. A progressão da doença leva ao comprometimento do osso adjacente o qual fica com fissuras e cistos.
Ao mesmo tempo, aparentemente como uma tentativa de aumentar a superfície de contato e procurando maior estabilidade, o osso prolifera. Mas não é um osso normal, sendo mais rígido e mais suscetível a microfraturas que ocorrem principalmente em articulações que suportam peso.
Aparentemente devido à reação inflamatória local todos os elementos da articulação sofrem hipertrofia: cápsula, tendões, músculos e ligamentos. As articulações sofrem aumento de volume e podem estar com calor local.
O grau de comprometimento é bastante variado. A doença pode evoluir até a destruição da articulação ou estacionar a qualquer momento. Há indivíduos que têm deformidades nos dedos e que nunca sentiram dor e outros que terão dor e progressiva piora da doença com conseqüentes deformidade e diminuição da função articular.
Não se conhece o gatilho inicial da Osteoartrite. Acredita-se que mecanismos diferentes levem às mesmas alterações na função e composição das estruturas articulares.
Freqüência
A doença torna-se evidente a partir dos 30 anos de idade. Estima-se que 35% das pessoas já tenha Osteoartrite (OA) em alguma articulação nesta idade, sendo a grande maioria sem sintomas. Joelhos e coluna cervical são os locais mais atingidos. Aos 50 anos aumenta muito a prevalência e a partir da década dos 70 anos 85% dos indivíduos terão alterações ao RX.
Fatores de risco
Osteoartrite (OA) nos dedos das mãos é mais freqüente em mulheres e tem grande incidência familiar, favorecendo um mecanismo genético.
Osteoartrite em articulações que recebem carga, como quadris e joelhos, são mais freqüentes em obesos o mesmo podendo acontecer com a coluna vertebral.
Defeitos posturais como pernas arqueadas ou pernas em xis favorecem Osteoartrite de joelhos. Posição inadequada do fêmur em relação à bacia leva à degeneração cartilaginosa em locais específicos da articulação coxo-femural.
Do mesmo modo, defeitos nos pés levarão à instalação de Osteoartrite, sendo o joanete o melhor modelo. Entretanto, há pacientes que sofrem outro tipo de OA no dedo grande do pé que não se relaciona com defeito postural.
Hiperelasticidade articular, mais comum em mulheres, pode permitir que as superfícies articulares ultrapassem seus limites anatômicos e a cartilagem, deslizando em superfícies duras, sofre erosão. Osteoartrite OA entre fêmur e rótula (femuropatelar) é um exemplo comum.
Doenças metabólicas como diabete e hipotireoidismo favorecem o desenvolvimento de Osteoartrite.
Outras doenças que afetam a cartilagem como artrite reumatóide, artrite infecciosa e doenças por depósitos de cristais (gota e condrocalcinose) podem apresentar-se com o mesmo tipo de lesão e são rotuladas como Osteoartrite (OA) secundária.
Manifestações clínicas
O que se sente?
Antes da dor, os pacientes com OA podem reclamar de desconforto articular ou ao redor das articulações e cansaço. Posteriormente, aparece dor e, mais tarde, deformidades e limitação da função articular. No início, a dor surge após uso prolongado ou sobrecarga das articulações comprometidas.
Mais tarde, os pacientes reclamam que após longo período de inatividade como dormir ou sentar-se por muito tempo em Osteoartrite de quadrís ou joelhos, há dor no início do movimento que permanece alguns minutos.
São exemplos a dor discreta com rigidez que dura alguns minutos nos dedos pela manhã e nos joelhos também de manhã ou após algum tempo sentado. Nos pacientes que têm piora progressiva a dor fica mais forte e duradoura e as deformidades acentuam-se.
Na Osteoartrite de quadrís e joelhos, subir e descer escadas fica mais difícil assim como caminhadas mais longas.
A inflamação pode produzir aumento do líquido intra-articular. Nestas situações a dor aumenta, os movimentos ficam mais limitados e a palpação articular evidencia calor local além da presença do derrame.
Acredita-se que só o fato de uma articulação estar comprometida já é suficiente para que se desenvolva atrofia muscular, mas certamente a falta de movimentos completos e a inatividade são fatores coadjuvantes importantes. Em casos extremos, os pacientes necessitam fazer uso de bengalas ou muletas. Raramente um paciente com Osteoartrite de quadris ou joelhos vai para cadeira-de-rodas.
Osteoartrite (OA) das mãos.
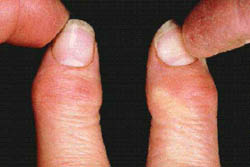
É mais freqüente em mulheres. Pode haver comprometimento exclusivo das articulações próximas às unhas (interfalangianas distais). Após lenta evolução que não obrigatoriamente acompanha-se de dor e vermelhidão estas articulações ficam com proeminências ósseas duras e de distribuição irregular.
Com menor freqüência, podem ocorrer lesões semelhantes nas articulações interfalangianas proximais. A capacidade de preensão pode ficar bastante comprometida.
Local comumente envolvido é a articulação abaixo do polegar (trapéziometacarpiana). Com freqüência esta articulação, em ambas mãos, é a única envolvida.
A gravidade é bastante variável. Pode não afetar a função das mãos mas há casos de deslocamento do polegar para a região palmar e dor forte ao segurar-se objetos.
Osteoartrite (OA) dos pés
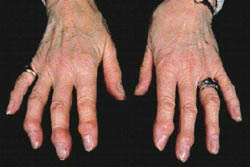
É comum o joanete. É o resultado de um defeito da posição dos ossos que formam a articulação do grande artelho com o médio-pé.
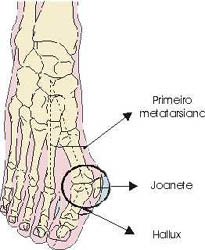
A Osteoartrite é conseqüente ao desgaste da cartilagem e do osso adjacente e conseqüente proliferação óssea anormal. Atrito provocado pelo uso de calçados forma uma bursa (cisto abaixo da pele) que inflama e dói.
Vários defeitos posturais ou da mecânica dos pés que não são corrigidos com calçados apropriados, exercícios, palmilhas ou cirurgia levam a lesões cartilaginosas e conseqüente OA. Os pés podem ficar bastante deformados e rígidos, dificultando a marcha e o uso de calçados.
Osteoartrite (OA) dos quadris (coxartrose)

A grande maioria das coxartroses é secundária a defeitos da bacia ou fêmur congênitos ou adquiridos precocemente.
Quando as duas articulações estão envolvidas, obesidade deve ser um fator importante. A dor pode localizar-se na virilha, nádega, parte externa ou interna da coxa e, menos freqüentemente, irradiar-se ou ser unicamente no joelho. Em todas as situações haverá progressiva limitação dos movimentos da coxa, sendo comum dificuldade para colocar calçados e vestir calças.
Cancro ou Câncer
O câncer não é uma doença única, e sim um conjunto de doenças. Entenda melhor e descubra os principais sintomas.
O câncer (para brasileiros) ou cancro (para os resto dos países lusófonos) é o termo usado para designar mais de 100 doenças diferentes, que apresentam em comum, o crescimento desordenado de células anormais que possuem capacidade de invadir tecidos e se espalhar para outras regiões do corpo através dos vasos.
COMO SURGE UM CÂNCER?
É um processo complicado, mas vou tentar escrever do jeito mais simples possível. Mais uma vez a descrição não será 100% exata, já que esse texto não é voltado para estudantes da área de saúde.
O ciclo básico de vida de uma célula é se multiplicar quando necessário e morrer quando se torna velha ou quando sofre alguma lesão na sua estrutura.
As nossas células são programas para se auto-destruírem em caso de alteração da sua conformação original, principalmente se houver lesão no DNA (código genético da célula, que determina suas características), não passível de reparo. Esta auto-destruição se chama apoptose. Este mecanismo evita que lesões no DNA possam ser perpetuadas através da multiplicação de células anômalas.
Lesões celulares ocorrem diariamente em nosso organismo e são amplificadas pelo cigarro, radiação e produtos químicos, todas substâncias com alto potencial de lesão do DNA (carcinógenos). Só o cigarro possui mais de 4000 substâncias comprovadamente carcinógenas.
Graças a apoptose, não desenvolvemos câncer a todo momento.
O processo de multiplicação celular e apoptose é controlado por um grupo de genes chamado de protooncogenes. São os genes supressores de tumor. O câncer começa a surgir quando ocorrem mutações nesses protooncogenes, fazendo com que suas funções sejam abolidas. Os genes alterados passam a se chamar oncogenes, e em vez de impedir a formação de tumores, passam a estimulá-los.
A partir desse momento as células com alterações estruturais não só conseguem se multiplicar, como estão protegidas da apoptose. Portanto, são células se proliferam rapidamente e não morrem. Estas são as células cancerígenas.
Existem vários tipos de protooncogenes, cada tipo de câncer está relacionado a um ou mais desses. Os diferentes tipos de oncogenes explicam porque algumas famílias apresentam tendência a desenvolverem alguns tipos de câncer e porque o cigarro causa câncer de pulmão em alguns, de boca em outros, de bexiga, rins etc... A ausência de ativação de oncognes específicos também explica porque alguns fumantes nunca desenvolvem câncer.
POR QUE O CÂNCER LEVA A MORTE ?
As células cancerígenas além de se multiplicarem, conseguem produzir seus próprios vasos sanguíneos, o que permite a elas receberem nutrientes e formarem as massas de células chamada de tumores. Outro fator determinante é a capacidade dessas células anômalas de alcançarem a circulação sanguínea e viajarem pelo corpo.
Quanto mais lesão tiver sofrido o DNA da célula, mais diferente ela será da célula que lhe deu origem. E se ela é diferente, não consegue despenhar as funções vitais que a original exerce. Então, passamos a ter um quadro onde células que não desempenham nenhuma função se multiplicam de modo muito mais rápido que o normal e passam não só a competir por alimento, como invadem e tomam o lugar das células normais.
Depois de um tempo passamos a ter um pulmão em que a maioria das células não consegue captar oxigênio, um intestino que não absorve nutrientes, um rim que não produz urina... Além disso, temos uma massa tumoral que cresce tanto que começa a esmagar e obstruir outros tecidos e vasos importantes. Um tumor do pescoço pode comprimir a traqueia e causar asfixia, um tumor de intestino obstrui a passagem das fezes, um tumor cerebral pode comprimir o cérebro contra o crânio etc...
A célula cancerígena tem a capacidade de invadir tecidos próximos e alcaçar vasos sanguíneos, podendo viajar pela circulação e acometer outros órgãos distantes. Este processo se chama metástase. Os tumores benignos são aqueles que não tem capacidade de metastizar.
Alguns termos para melhor compreesão:
- Câncer - São células anômalas com capacidade de multiplicação, invasão a distância e de destruição. O câncer é sempre maligno.
- Tumor - É o aumento anormal de um tecido, pode ser maligno ser for criado por células cancerígenas, mas pode ser benigno se for por células sem características de câncer.
- Neoplasia - Semelhante a tumor.
- Carcinoma - Câncer originado das células epiteliais (tipo de células que recobre a pele e a maioria dos órgãos).
- Sarcoma - Câncer originado de células de músculos, gordura, osso e cartilagem.
- Leucemia - Câncer que se origina de células do sangue na medula óssea.
- Linfoma - Câncer que se origina das células de defesa do organismo
QUAIS OS SINTOMAS DO CÂNCER ?
Como eu já disse, existem vários tipos de câncer, e cada um tem sua apresntação clínica distinta. Um tumor cerebral tem sintomas completamente diferentes de um tumor de próstata.
Porém, os cÂnceres apresentam um grupo de sinais e sintomas que são mais ou mesnos comuns a todos.
DOR
É conhecido de todos que doentes com câncer sofrem de dores crônicas. Mas por que isso acontece?A maioria das dores do cânceres são de origem óssea, principalmente pelas metástases. Qualquer tumor pode metastizar para os ossos, e doentes em fases terminais podem apresentar várias fraturas espontâneas pelo corpo. A cefaléia (dor de cabeça) também é um sintoma comum e pode ocorrer por metástases para o crânio, compressão do cérebro pelo tumor, lesões hemorrágicas ou compressão dos nervos faciais. A compressão de nervos periféricos pela massa tumoral pode ser causa de dor em qualquer local do corpo. A dor também pode ser um efeito colateral da quimioterapia e da radioterapia.
CAQUEXIA
A caquexia é uma diminuição do apetite associado a rápida perda de peso e massa muscular. Diferente da desnutrição comum, a caquexia se caracteriza por uma perda de peso desproporcional a falta de ingestão calórica, que normalmente não é corrigida mesmo com uma alimentação forçada.As células tumorais produzem substâncias que agem diretamente no tecido muscular e adiposo (gorduroso), levando ao seu consumo. Por isso, doentes com câncer apresentam tanta dificuldade em ganhar peso.
FADIGA
O cansaço crônico do doente neoplásico pode ser causado pela própria caquexia, por anemia, por dificuldade em dormir (normalmente pela dor), e pela ação direta de substâncias produzidas pelo tumor.Também pode ser um efeito secundário do tratamento.
ANEMIA
A anemia é um achado quase universal nos cânceres. Qualquer doença crônica pode causar uma inibição na produção de hemácias pela medula óssea, e o câncer não é diferente. A anemia pode ser também por sangramentos do tumor, por inibição da absorção de ferro, por invasão tumoral da medula óssea ou por ação direta da quimioterapia e da radioterapia.
TROMBOSE
Pacientes com tumores malígnos tendem a apresentar um estado de hipercoagulabilidade, ou seja, o sangue inapropriadamente coagula dentro do próprio vaso, formando trombos (leia sobre trombos no texto sobre AVE).Pode haver trombose de artérias e veias, assim como uma síndrome gravíssima chamada de "coagulação intravascular disseminada" (CIVD), onde a cascata da coagulação começa a ser ativada no corpo todo ao mesmo tempo, levando a formação simultânea de trombos e hemorragias difusas.
A ocorrência de trombose pode ser o primeiro sinal de uma neoplasia, e às vezes, antecede o diagnóstico de câncer em vários meses.
Cirrose hepática
Cirrose hepática e regeneração
O tipo mais comum de cirrose, a cirrose hepática, afeta o fígado e surge devido ao processo crônico e progressivo de inflamações (hepatites), fibrose e por fim ocorre a formação de múltiplos nódulos, que caracterizam a cirrose. A cirrose é considerada uma doença terminal do fígado para onde convergem diversas doenças diferentes, levando a complicações decorrentes da destruição de suas células, da alteração da sua estrutura e do processo inflamatório crônico. A capacidade regenerativa do fígado é conhecida e até faz parte da mitologia grega. É possível retirar cirurgicamente mais de dois terços de um fígado normal e a porção restante tende a crescer até praticamente o tamanho normal, com um processo de multiplicação celular que se inicia logo nas primeiras 24 horas, através de mecanismo ainda não bem esclarecido (o mesmo acontece com o transplante hepático intervivos, em que o receptor recebe uma porção do fígado do doador e depois ambos crescem). No entanto, a cirrose é o resultado de um processo crônico de destruição e regeneração com formação de fibrose. Nessa fase da hepatopatia, a capacidade regenerativa do fígado é mínima.
Causas
Fígado normal
Apesar da crença popular de que a cirrose hepática é uma doença de alcoólatras, todas as doenças que levam a inflamação crônica do fígado (hepatopatia crônica) podem desenvolver essa patologia:
* Hepatite autoimune
* Lesão hepática induzida por drogas ou toxinas
* Lesão hepática induzida pelo álcool
* Hepatites virais B, C e D
* Doenças metabólicas
o Deficiência de alfa-1-antitripsina
o Doença de Wilson
o Hemocromatose
* Distúrbios vasculares
o Insuficiência cardíaca direita crônica
o Síndrome de Budd-Chiari
* Cirrose biliar
o Cirrose biliar primária
o Cirrose biliar secundária a obstrução crônica
o Colangite esclerosante primária
* Atresia biliar
* Insuficiência congênita de ductos intra-hepáticos (Síndrome de Alagille)
* Cirrose criptogênica (causa desconhecida)
Sintomas
Cirrose
No início não há praticamente nenhum sintoma, o que a torna de difícil diagnóstico precoce, pois a parte ainda saudável do fígado consegue compensar as funções da parte lesada durante muito tempo. Numa fase mais avançada da doença, podem surgir desnutrição, hematomas, aranhas vasculares, sangramentos de mucosas (especialmente gengivas), icterícia ("amarelão"), ascite ("barriga-d'água"), hemorragias digestivas (por diversas causas, entre elas devido a rompimento de varizes no esófago,levando o doente a expelir sangue pela boca e nas fezes) e encefalopatia hepática (processo causado pelo acúmulo de substâncias tóxicas que leva a um quadro neurológico que pode variar entre dificuldade de atenção e coma).
Tratamento
O único tratamento totalmente eficaz para portadores de cirrose hepática é o transplante de fígado, mas também pode haver melhoras se for suspenso o agente agressor que originou a cirrose, como o álcool ou o vírus da hepatite. Como o transplante está indicado apenas em situações aonde o risco do procedimento é inferior ao risco esperado sem o procedimento, se não houver indicação de transplante deve-se manter acompanhamento médico periódico para a detecção precoce de complicações como desnutrição, ascite, varizes esôfago-gastricas, hepatocarcinoma, procedendo-se intervenção, se necessária.
Diabetes insipidus
O hormônio diurético é produzido normalmente no hipotálamo do cérebro e libertado pela neuro-hipófise. Ele controla o modo como os rins removem, filtram e reabsorvem fluidos dentro da corrente sanguínea. Quando ocorre a falta desse hormônio (ou quando os rins não podem responder ao hormônio) os fluidos passam pelos rins e se perdem por meio da micção. Assim, uma pessoa com diabetes insípido precisa ingerir grande quantidade de água em resposta à sede extrema para compensar a perda de água.
Índice[esconder] |
[editar] Sinais e sintomas
A diurese excessiva e a sede intensa são típicos da DI. Os sintomas da diabetes insipidus são similares aos da diabetes mellitus, com a distinção de que não ocorre a glicosúria (urina doce) e não há hiperglicemia (glicose do sangue elevada). Problemas de visão são raros.
O excesso de diurese continua dia e noite. Em crianças, a DI pode interferir no apetite, no ganho de peso e no crescimento. Ela pode levar à febre, vómitos ou diarreia. Adultos com uma DI sem tratamento permanecem saudáveis por décadas desde que a ingestão de água seja suficiente para compensar as perdas urinárias. Entretanto, há um risco contínuo de desidratação.
[editar] Diagnóstico
Para identificação da causa da poliúria, a glicemia (glicose do sangue) e o cálcio sérico devem ser testados. Os eletrólitos podem se mostrar alterados; hipernatremia (excesso de sódio) são comuns nos casos graves. O exame Parcial de Urina mostra baixos níveis de electrólitos, e a osmolaridade e densidade urinárias são baixas.
Um "teste de privação de água" ajuda a determinar se a DI é causada por:
- excesso de ingestão de líquidos;
- um defeito na produção do Hormônio Antidiurético; ou
- um defeito na resposta renal ao hormônio.
Este teste mede modificações no peso corporal, volume urinário e composição urinária. Dosagens de Hormônio Antidiurético (ADH) no sangue pode ser necessário para o diagnóstico final.
Para distinguir entre as várias formas, a estimulação com desmopressina (um análogo mais potente da vasopressina), pode também ser utilizada, injectável, via spray nasal ou via oral. Caso ocorra redução do volume urinário e aumento da densidade urinária a produção do ADH pela glândula pituitária é deficiente e a resposta renal é normal. Caso haja falta de resposta renal a desmopressina não fará efeito.
Se a DI central é suspeitada, testa-se outro hormónios produzidos pela pituitária e realiza-se uma ressonância nuclear magnética (MRI) para descobrir se alguma outra doença está afectando a pituitária, como um prolactinoma.
[editar] Patofisiologia
A homeostase requer que a pressão arterial e os níveis séricos de sódio e potássio estejam dentro de uma estreita faixa de variação. Em geral esta regulagem é feita pelos rins e o DI pode afectar profundamente estes níveis.
Há várias formas de Diabetes Insipidus:
- DI Central causada pelo dano ao hipotálamo resultante de cirurgia, infecção, tumor ou acidentes vasculares encefálicos. É a condição mais comum.
- DI Nefrogenico quando o rim está lesado. Esta é uma condição rara.
- DI Dipsogenico é causado por um defeito no mecanismo da sede, por um defeito no hipotálamo. Este defeito aumenta a ingestão de água através de uma sede anormal.
- DI Gestacional , que ocorre na gravidez.
[editar] Tratamento
A DI Central e a DI gestacional respondem ao uso de desmopressina. Na DI dipsogenica e na DI nefrogênica a desmopressina não surte efeito. No entanto, o uso de diuréticos como a hidroclorotiazida pode melhorar a hiperalemia.
Diabetes mellitus
DIABETES MELLITUS ( DM )
O que é ?
Doença provocada pela deficiência de produção e/ou de ação da insulina, que leva a sintomas agudos e a complicações crônicas características.
O distúrbio envolve o metabolismo da glicose, das gorduras e das proteínas e tem graves conseqüências tanto quando surge rapidamente como quando se instala lentamente. Nos dias atuais se constitui em problema de saúde pública pelo número de pessoas que apresentam a doença, principalmente no Brasil.
Apresenta diversas formas clínicas, sendo classificado em:
| Diabetes Mellitus tipo I: Ocasionado pela destruição da célula beta do pâncreas, em geral por decorrência de doença auto-imune, levando a deficiência absoluta de insulina. | |
| Diabetes Mellitus tipo II: Provocado predominantemente por um estado de resistência à ação da insulina associado a uma relativa deficiência de sua secreção. | |
| Outras formas de Diabetes Mellitus: quadro associado a desordens genéticas, infecções, doenças pancreáticas, uso de medicamentos, drogas ou outras doenças endócrinas. | |
| Diabetes Gestacional: Circunstância na qual a doença é diagnosticada durante a gestação, em paciente sem aumento prévio da glicose. |
Como se desenvolve?
Conforme pode ser observado no item acima (formas clínicas), são várias as causas do DM.
No DM tipo I, a causa básica é uma doença auto-imune que lesa irreversivelmente as células pancreáticas produtoras de insulina (células beta). Assim sendo, nos primeiros meses após o início da doença, são detectados no sangue dos pacientes, diversos anticorpos sendo os mais importantes o anticorpo anti-ilhota pancreática, o anticorpo contra enzimas das células beta (anticorpos antidescarboxilase do ácido glutâmico - antiGAD, por exemplo) e anticorpos anti-insulina.
No DM tipo II, ocorrem diversos mecanismos de resistência a ação da insulina, sendo o principal deles a obesidade, que está presente na maioria dos pacientes.
Nos pacientes com outras formas de DM, o que ocorre em geral é uma lesão anatômica do pâncreas, decorrente de diversas agressões tóxicas seja por álcool, drogas, medicamentos ou infecções, entre outras.
O que se sente ?
Os sintomas do DM são decorrentes do aumento da glicemia e das complicações crônicas que se desenvolvem a longo prazo.
Os sintomas do aumento da glicemia são:
| sede excessiva | |
| aumento do volume da urina, | |
| aumento do número de micções | |
| surgimento do hábito de urinar à noite | |
| fadiga, fraqueza, tonturas | |
| visão borrada | |
| aumento de apetite | |
| perda de peso. |
Estes sintomas tendem a se agravar progressivamente e podem levar a complicações severas que são a cetoacidose diabética (no DM tipo I) e o coma hiperosmolar (no DM tipo II).
Os sintomas das complicações envolvem queixas visuais, cardíacas, circulatórias, digestivas, renais, urinárias, neurológicas, dermatológicas e ortopédicas, entre outras.
| Sintomas visuais: O paciente com DM descompensado apresenta visão borrada e dificuldade de refração. As complicações a longo prazo envolvem diminuição da acuidade visual e visão turva que podem estar associadas a catarata ou a alterações retinianas denominadas retinopatia diabética. A retinopatia diabética pode levar ao envolvimento importante da retina causando inclusive descolamento de retina, hemorragia vítrea e cegueira. | |
| Sintomas cardíacos: Pacientes diabéticos apresentam uma maior prevalência de hipertensão arterial, obesidade e alterações de gorduras. Por estes motivos e, principalmente se houver tabagismo associado, pode ocorrer doença cardíaca. A doença cardíaca pode envolver as coronárias, o músculo cardíaco e o sistema de condução dos estímulos elétricos do coração. Como o paciente apresenta em geral também algum grau de alteração dos nervos do coração, as alterações cardíacas podem não provocar nenhum sintoma, sendo descobertas apenas na presença de sintomas mais graves como o infarto do miocárdio, a insuficiência cardíaca e as arritmias. | |
| Sintomas circulatórios: Os mesmos fatores que se associam a outras complicações tornam mais freqüentes as alterações circulatórias que se manifestam por arteriosclerose de diversos vasos sangüíneos. São freqüentes as complicações que obstruem vasos importantes como as carótidas, a aorta, as artérias ilíacas, e diversas outras de extremidades. Essas alterações são particularmente importantes nos membros inferiores (pernas e pés), levando a um conjunto de alterações que compõem o "pé diabético". O "pé diabético" envolve, além das alterações circulatórias, os nervos periféricos (neuropatia periférica), infecções fúngicas e bacterianas e úlceras de pressão. Estas alterações podem levar a amputação de membros inferiores, com grave comprometimento da qualidade de vida. | |
| Sintomas digestivos: Pacientes diabéticos podem apresentar comprometimento da inervação do tubo digestivo, com diminuição de sua movimentação, principalmente em nível de estômago e intestino grosso. Estas alterações podem provocar sintomas de distensão abdominal e vômitos com resíduos alimentares e diarréia. A diarréia é caracteristicamente noturna, e ocorre sem dor abdominal significativa, freqüentemente associado com incapacidade para reter as fezes (incontinência fecal). | |
| Sintomas renais: O envolvimento dos rins no paciente diabético evolui lentamente e sem provocar sintomas. Os sintomas quando ocorrem em geral já significam uma perda de função renal significativa. Esses sintomas são: inchume nos pés (edema de membros inferiores), aumento da pressão arterial, anemia e perda de proteínas pela urina (proteinúria). | |
| Sintomas urinários: Pacientes diabéticos podem apresentar dificuldade para esvaziamento da bexiga em decorrência da perda de sua inervação (bexiga neurogênica). Essa alteração pode provocar perda de função renal e funcionar como fator de manutenção de infecção urinária. No homem, essa alteração pode se associar com dificuldades de ereção e impotência sexual, além de piorar sintomas relacionados com aumento de volume da próstata. | |
| Sintomas neurológicos: O envolvimento de nervos no paciente diabético pode provocar neurites agudas (paralisias agudas) nos nervos da face, dos olhos e das extremidades. Podem ocorrer também neurites crônicas que afetam os nervos dos membros superiores e inferiores, causando perda progressiva da sensibilidade vibratória, dolorosa, ao calor e ao toque. Essas alterações são o principal fator para o surgimento de modificações na posição articular e de pele que surgem na planta dos pés, podendo levar a formação de úlceras ("mal perfurante plantar"). Os sinais mais característicos da presença de neuropatia são a perda de sensibilidade em bota e luva, o surgimento de deformidades como a perda do arco plantar e as "mãos em prece" e as queixas de formigamentos e alternância de resfriamento e calorões nos pés e pernas, principalmente à noite. | |
| Sintomas dermatológicos: Pacientes diabéticos apresentam uma sensibilidade maior para infecções fúngicas de pele (tinha corporis, intertrigo) e de unhas (onicomicose). Nas regiões afetadas por neuropatia, ocorrem formações de placas de pele engrossada denominadas hiperceratoses, que podem ser a manifestação inicial do mal perfurante plantar. | |
| Sintomas ortopédicos: A perda de sensibilidade nas extremidades leva a uma série de deformidades como os pés planos, os dedos em garra, e a degeneração das articulações dos tornozelos ou joelhos ("Junta de Charcot"). |
Como o médico faz o diagnóstico ?
O diagnóstico pode ser presumido em pacientes que apresentam os sintomas e sinais clássicos da doença, que são: sede excessiva, aumento do volume e do número de micções (incluindo o surgimento do hábito de acordar a noite para urinar), fome excessiva e emagrecimento. Na medida em que um grande número de pessoas não chega a apresentar esses sintomas, durante um longo período de tempo, e já apresentam a doença, recomenda-se um diagnóstico precoce .
O diagnóstico laboratorial do Diabetes Mellitus é estabelecido pela medida da glicemia no soro ou plasma, após um jejum de 8 a 12 horas. Em decorrência do fato de que uma grande percentagem de pacientes com DM tipo II descobre sua doença muito tardiamente, já com graves complicações crônicas, tem se recomendado o diagnóstico precoce e o rastreamento da doença em várias situações. O rastreamento de toda a população é porém discutível.
Fatores de Risco para o Diabetes Mellitus
Existem situações nas quais estão presentes fatores de risco para o Diabetes Mellitus, conforme apresentado a seguir:
| Idade maior ou igual a 45 anos | |
| História Familiar de DM ( pais, filhos e irmãos) | |
| Sedentarismo | |
| HDL-c baixo ou triglicerídeos elevados | |
| Hipertensão arterial | |
| Doença coronariana | |
| DM gestacional prévio | |
| Filhos com peso maior do que 4 kg, abortos de repetição ou morte de filhos nos primeiros dias de vida | |
| Uso de medicamentos que aumentam a glicose ( cortisonas, diuréticos tiazídicos e beta-bloqueadores) |
Objetivos do Tratamento
Os objetivos do tratamento do DM são dirigidos para se obter uma glicemia normal tanto em jejum quanto no período pós-prandial, e controlar as alterações metabólicas associadas.
Tratamento
O tratamento do paciente com DM envolve sempre pelos menos 4 aspectos importantes:
| Plano alimentar: | É o ponto fundamental do tratamento de qualquer tipo de paciente diabético. O objetivo geral é o de auxiliar o indivíduo a fazer mudanças em seus hábitos alimentares, permitindo um controle metabólico adequado. Além disso, o tratamento nutricional deve contribuir para a normalização da glicemia, diminuir os fatores de risco cardiovascular, fornecer as calorias suficientes para manutenção de um peso saudável, prevenir as complicações agudas e crônicas e promover a saúde geral do paciente. Para atender esses objetivos a dieta deveria ser equilibrada como qualquer dieta de uma pessoa saudável normal, sendo individualizada de acordo com as particularidades de cada paciente incluindo idade, sexo, situação funcional, atividade física, doenças associadas e situação sócioeconômico-cultural. Composição do plano alimentar A composição da dieta deve incluir 50 a 60% de carboidratos, 30% de gorduras e 10 a 15% de proteínas. Os carboidratos devem ser preferencialmente complexos e ingeridos em 5 a 6 porções por dia. As gorduras devem incluir no máximo 10% de gorduras saturadas, o que significa que devem ser evitadas carnes gordas, embutidos, frituras, laticínios integrais, molhos e cremes ricos em gorduras e alimentos refogados ou temperados com excesso de óleo. As proteínas devem corresponder a 0,8 a 1,0 g/kg de peso ideal por dia, o que corresponde em geral a 2 porções de carne ao dia. Além disso, a alimentação deve ser rica em fibras, vitaminas e sais minerais, o que é obtido pelo consumo de 2 a 4 porções de frutas, 3 a 5 porções de hortaliças, e dando preferência a alimentos integrais. O uso habitual de bebidas alcoólicas não é recomendável, principalmente em pacientes obesos, com aumento de triglicerídeos e com mau controle metabólico. Em geral podem ser consumidos uma a duas vezes por semana, dois copos de vinho, uma lata de cerveja ou 40 ml de uísque, acompanhados de algum alimento, uma vez que o álcool pode induzir a queda de açúcar (hipoglicemia). | |
| Atividade física: | Todos os pacientes devem ser incentivados à pratica regular de atividade física, que pode ser uma caminhada de 30 a 40 minutos ou exercícios equivalentes. A orientação para o início de atividade física deve incluir uma avaliação médica adequada no sentido de avaliar a presença de neuropatias ou de alterações cardio-circulatórias que possam contra-indicar a atividade física ou provocar riscos adicionais ao paciente. | |
| Medicamentos, Hipoglicemiantes orais: | São medicamentos úteis para o controle de pacientes com DM tipo II, estando contraindicados nos pacientes com DM tipo I. Em pacientes obesos e hiperglicêmicos, em geral a medicação inicial pode ser a metformina, as sultoniluréias ou as tiazolidinedionas. A insulina é a medicação primordial para pacientes com DM tipo I, sendo também muito importante para os pacientes com DM tipo II que não responderam ao tratamento com hipoglicemiantes orais. | |
| Rastreamento: | O rastreamento, a detecção e o tratamento das complicações crônicas do DM deve ser sempre realizado conforme diversas recomendações. Essa abordagem está indicada após 5 anos do diagnóstico de DM tipo I, no momento do diagnóstico do DM tipo II, e a seguir anualmente. Esta investigação inclui o exame de fundo de olho com pupila dilatada, a microalbuminúria de 24 horas ou em amostra, a creatinina sérica e o teste de esforço. Uma adequada analise do perfil lipídico, a pesquisa da sensibilidade profunda dos pés deve ser realizada com mofilamento ou diapasão, e um exame completo dos pulsos periféricos dever ser realizada em cada consulta do paciente. Uma vez detectadas as complicações existem tratamentos específicos, os quais serão melhor detalhados em outros artigos desse site. |
Como se previne ?
A prevenção do DM só pode ser realizada no tipo II e nas formas associadas a outras alterações pancreáticas. No DM tipo I, na medida em que o mesmo se desenvolve a partir de alterações auto-imunes, essas podem ser até mesmo identificadas antes do estado de aumento do açúcar no sangue. Esse diagnóstico precoce não pode ser confundido porém com prevenção, que ainda não é disponível.
No DM tipo II, na medida em que uma série de fatores de risco são bem conhecidos, pacientes que sejam portadores dessas alterações podem ser rastreados periodicamente e orientados a adotarem comportamentos e medidas que os retire do grupo de risco.
Assim é que pacientes com história familiar de DM, devem ser orientados a:
| manter peso normal | |
| praticar atividade física regular | |
| não fumar | |
| controlar a pressão arterial | |
| evitar medicamentos que potencialmente possam agredir o pâncreas (cortisona, diuréticos tiazídicos) |